卵巢作为女性重要内生殖器官,接受来自中枢神经系统-下丘脑-垂体-卵巢的复杂调控, 完成分泌激素维持女性体征和排卵功能。
卵巢早衰(POF)是指女性在40周岁以前,除妊娠外,由某种原因导致闭经,以血清雌激素水平下降、促性腺激素水平升高为特征的疾病,在育龄女性中发病率超过1%,且近年来发病率呈上升和年轻化趋势,被认为是导致不孕的“不治之症”。卵巢早衰的女性即使通过辅助生殖技术也很难实现受孕,因为这类患者在月经周期中没有优势卵泡活动,无法取得卵子。
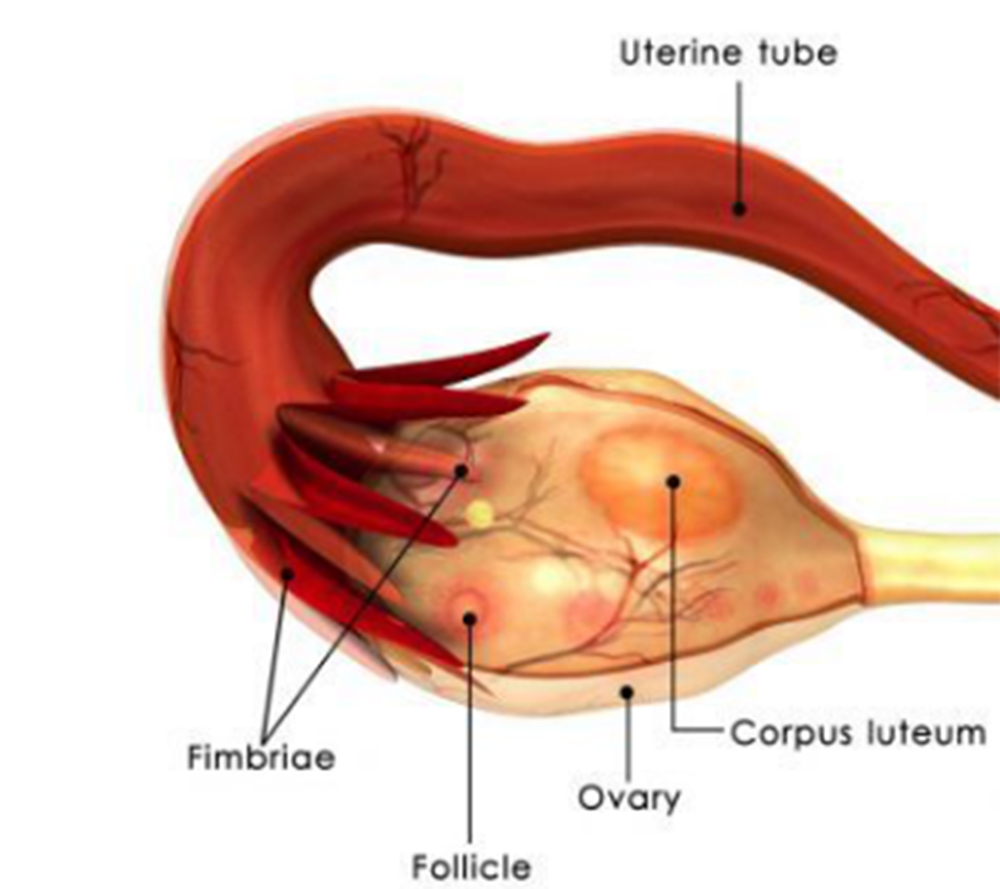
传统方法干预卵巢早衰效果不尽人意
目前被广为接受临床诊断标准为:女性40 周岁以前出现至少4个月闭经,卵泡期血清检测2次或以上(2 次检查间隔不少于1个月)均提示血清FSH水平>40 U/L,常伴有雌二醇 <73.2 pmol/L。
卵巢早衰临床常规干预方法包括雌孕激素替代、促排卵治疗、免疫干预以及卵巢移植等,虽然具有一定缓解作用,但无法达到预期效果。
干细胞疗法诸多优点为干预卵巢早衰提供新思路
随着再生医疗快速发展,目前干细胞在卵巢早衰领域应用被人们关注。干细胞是一种具有自我更新、不断增殖和多向分化潜能的细胞。
干细胞具有多分化潜能及低免疫源特性,取材方便,体外培养增殖容易,在维持机体内环境稳定、衰老、组织损伤修复及调节炎症性疾病中发挥重要作用。
干细胞还具有高增殖潜力,自我更新潜力、多向分化潜能,有造血支持、免疫调节和组织修复等优点,大量研究已证明干细胞可改善卵巢结构和功能,成为干预卵巢早衰较好办法。
临床研究证实干细胞疗法能够恢复卵巢功能
近年来,科学家研究发现,进入卵巢的干细胞除了能避开免疫系统“袭击”,还能够通过分泌多种生长因子调节T细胞,改善炎症环境减少卵泡凋亡,恢复卵巢功能并增加雌激素释放。
研究者在卵巢早衰小鼠模型中移植干细胞后,结果显示,小鼠卵泡凋亡减少,卵巢功能恢复,性激素水平升高。
研究还发现,同理通过观察大鼠模型发现,移植干细胞后第15、22、29天,大鼠的卵泡刺激素水平下降,雌二醇等激素水平上升,卵巢储备功能和卵泡数量逐渐完善。
除此之外,干细胞分泌成纤维生长因子2对受损卵巢有保护作用的同时还能减少颗粒细胞的凋亡;且干细胞还能帮助纤维细胞增殖,减少细胞外基质沉积,从而起到抗卵巢纤维化作用。
干细胞疗法有效干预卵巢早衰六种机制
上述动物实验研究表明,移植干细胞后造模动物卵巢形态、大小及动情周期均得到一定程度恢复,病理组织切片上可以观察到卵巢各级卵泡数明显增加,颗粒细胞生长,抗颗粒细胞凋亡,内分泌功能得到改善与恢复受孕等。
1、旁分泌:干细胞可分泌多种细胞因子(如血管内皮生长因子、肝细胞生长因子、类胰岛素一号增长因子等),抑制细胞凋亡,修复受损组织细胞。
2、归巢性:干细胞定植于受损伤部位并进行分化,部分补偿或替代修复其功能。
3、免疫调节:干细胞通过免疫调节作用,抑制机体免疫反应,促进受损组织自身修复。
4、抗纤维化:干细胞可通过修复卵巢间质防止卵巢纤维化,从而对受损卵巢起到保护作用。
5、多向分化潜力:干细胞进入损伤卵巢后可能直达损伤部位,并分化成部分血管内皮细胞,提供营养支。
6、调控作用:干细胞可改变部分基因表达,并通过基因改变达到调控卵巢功能的作用。
干细胞临床研究初获成果
我国率先开展脐带间充质干细胞干预卵巢早衰合并不孕症临床研究,该临床研究在通过医院伦理审查、国家卫计委备案后,成为我国实行干细胞临床研究备案制度后首批备案的8个干细胞临床研究项目之一。
自2015年首位受试者入组,经临床治疗术后复查,卵巢血流有明显改善,其后又先后进行了两次移植。两年过后受试者经检查确认大卵泡活动,实现自然受孕,其后顺利诞一名健康男婴。几年来,该临床研究已入组患者23人,随访发现9位患者有优势卵泡活动,已有2位患者获得临床妊娠,另有2位患者已经获得可移植胚胎,正在准备子宫内膜等待移植。攻克卵巢早衰合并不孕症标志着我国在卵巢再生临床研究中获得突破性进展,该科研成果宣告了再生医学技术攻克生殖系统“不治之症”的阶段性胜利。
随着干细胞技术的更快发展,相信我们能听到越来越多卵巢早衰患者通过干细胞疗法干预后顺利诞下健康宝宝的报道。
综上所述,干细胞疗法近年来在干预卵巢早衰取得叹为观止的效果,具有广阔临床转化应用前景。相信随着干细胞研究不断深入,它将为更多疑难杂症干预提供新方向。
