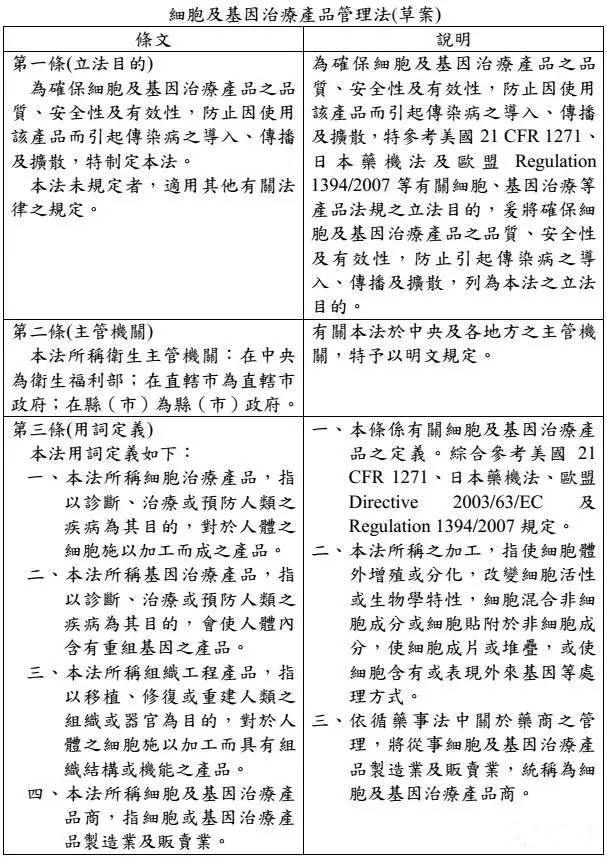
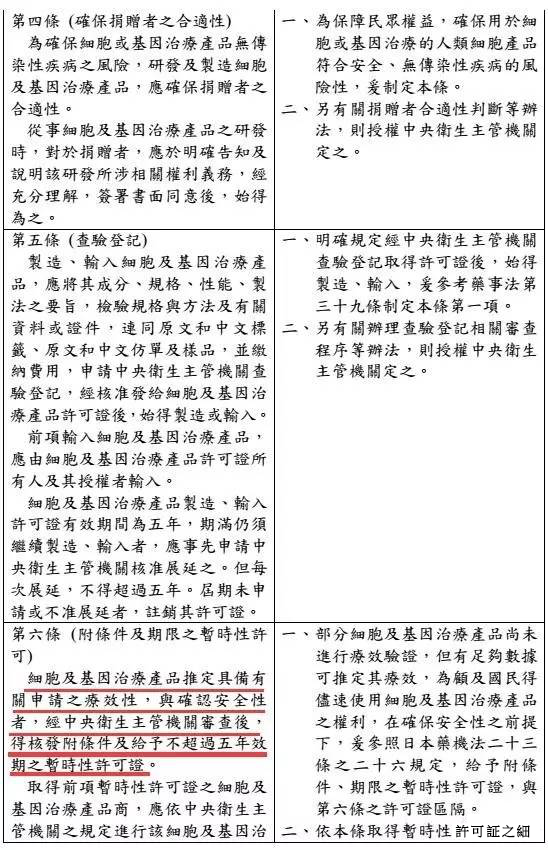
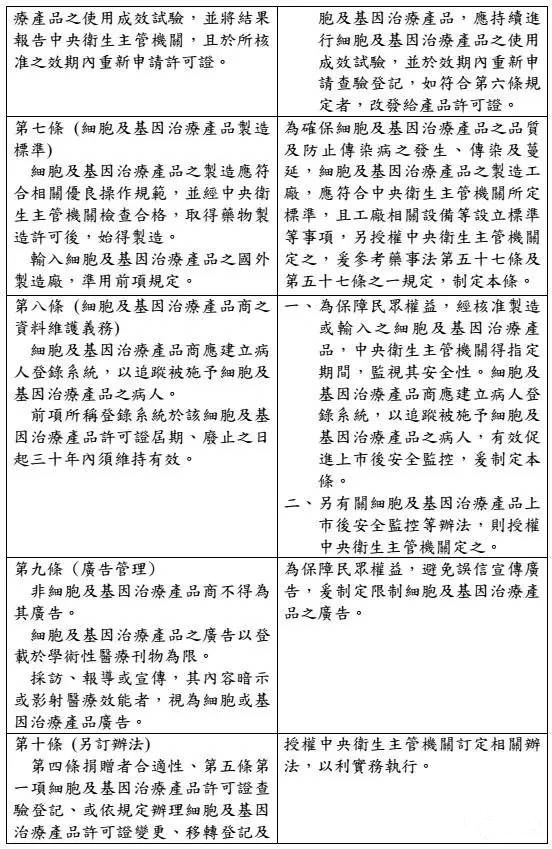
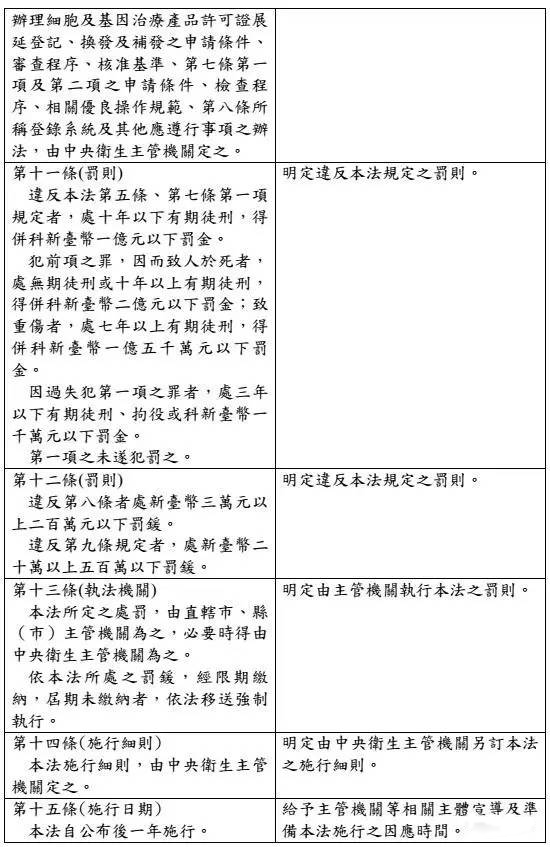
台湾食药署发布「细胞及基因治疗产品管理法」草案,明定细胞及基因治疗产品的定义,并规范捐赠者合适性,另也在确保安全状况下核淮暂时性许可证,给癌症末期、无药可医的患者治疗希望,预计草案将于年底前送行政院。
另,细胞与基因治疗要上市必须通过三期临床试验,并通过审核,但有些患者情况紧急,因此设定出暂时性许可证机制,只要确认捐赠者合适性,并使细胞或基因治疗产品无传染性疾病的风险、确保安全性的前提,不一定要完成三期试验也能核淮暂时许可使用。
新法规最大鬆绑之处,在于新设立「暂时许可」机制,祁若凤指出,为抢救生命,未来只要生命垂危的病人有需要,且又符合为新兴产品当初临床实验的对象,即使还没完成所有临床实验,食药署仍会给予暂时许可、提供病人救命使用。